写在前面:这一篇来讲讲Western blot。Western blot算是检测蛋白的gold standard吧,原理说起来是挺简单的,就是分离蛋白然后抗体给它显出来,但实际操作起来步骤多又繁琐,一个步骤出错就可能导致没结果,两三天的工作直接白干😵。所以这一篇就好好讲讲Western blot的每个步骤以及要注意的事项。
Reagent Preparation
做Western blot之前当然要先把各种要用到的溶液给配好了,包括制作gel需要的1.5 M Tris-HCl (pH=8.8),0.5 M Tris-HCl (pH=6.8);裂解细胞要用的lysis buffer;跑gel的loading dye,running buffer;转膜的transfer buffer;洗膜的washing buffer。。。把这些东东配好就是Western blot成功的前提😇
其中running buffer, transfer buffer, washing buffer因为用量大,所以每次都是配一桶8L全实验室共用的,其他的reagent就都是自己配的了。
配方如下:
• 1.5 M Tris-HCl (pH=8.8):91g Tris base + 400ml ddH2O → 加HCl调pH到8.8 → 加ddH₂O到500ml
• 0.5 M Tris-HCl (pH=6.8):30g Tris base + 400ml ddH2O → 加HCl调pH到6.8 → 加ddH₂O到500ml
• Lysis buffer:20ml 1.0 M Tris (pH=8.0) + 12ml 5.0 M NaCl + 1g Sodium Deoxycholate + 4ml 10% SDS + 4ml NP-40 → 加ddH₂O到400ml
• Loading dye:200.0 mM Tris-Cl (pH=6.8), 400.0 mM DDT (can skip adding this if 2-mercaptoethanol is used), 8.0% SDS, 0.4% Bromophenol Blue, 40.0% Glycerol
Protein Extraction
既然是检测蛋白,当然要先把protein给extract出来了,裂解细胞有不同的方法,我们实验室用的是sonication(声波裂解法)来裂解细胞,这里就讲讲这种方法。
首先,细胞收起来后我一般先用PBS洗一遍,这样把medium洗掉就感觉干净些😂接着就加lysis buffer和protease inhibitor (PI),PI的作用是防止蛋白降解,一般配成25×的PI,然后要用的时候lysis buffer和PI按24:1的比例加。Lysis buffer和PI的量取决于cell pellet的大小,如果细胞多点可能五六百μl,少点可能两三百μl,这就得看经验了,不然准备出来的蛋白浓度可能过高或过低。Lysis buffer和PI加到细胞后就可以拿去sonication了💢。
Sonication之前要先关好门戴上耳机🎧,因为这玩意儿声音非常刺耳。Sonication也是有技巧的,把sonicator伸到sample里面不能太靠近液面,不然sample马上就变成一管泡沫🤯,也不能乱晃,因为会碰到管壁。所以最好是把sonicator伸到液体底部,手要拿稳不碰壁🧪。Cell pellet大的话我一般会sonicate久点,三四十秒甚至一分钟,但问题是sonication的过程会产生热量,会导致裂解出来的蛋白变性,所以肯定不能一次性拿着sonicate三四十秒的。一个sample我一般会sonicate几秒钟,放回冰上,先去sonicate其他sample,等凉下来了再又sonicate,直到每个sample总时长达标。我个人有个习惯,就是加200μl lysis buffer就sonicate20秒,300就30秒,400就40秒,虽然也不绝对但有点参考价值吧📝。
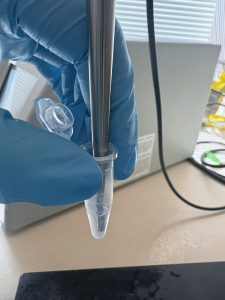
图为我正在进行sonication,手千万要拿稳了🤌每换一个sample都得拿酒精喷一喷,擦干,不然就cross contaminate了
Sonication完之后就是离心,把细胞裂完后的杂质给去除掉,这个离心要狠点,我一般是调18000rpm十分钟,这样应该能把杂质给离心出来了,然后把上清液移到新管里就算完成protein extration了,接着就可以冻上(-20℃)或者去量蛋白浓度了。
Protein Concentration and Sample Preparation
Western blot之前还得先量好蛋白的浓度,这样确保跑的时候每个sample加的蛋白量是一样的🧪。量蛋白是用BCA assay量的,具体讲就是BCA和铜离子会和蛋白反应,用颜色变化来确定蛋白浓度。
要量蛋白浓度前首先的先配置一组Standard,就是不同确定浓度的蛋白(用BSA,Bovine Serum Albumin),之后系统量吸光度的时候会根据Standard所生成的曲线来确定所量蛋白的浓度,Standard配方如下:
| Final Concentration (μg/μl) | μl of 2μg/μl of BSA | μl of water added |
|---|---|---|
| 1.5 | 150 | 50 |
| 1 | 100 | 100 |
| 0.5 | 50 | 150 |
| 0.2 | 20 | 180 |
| 0.1 | 10 | 190 |
| 0.05 | 5 | 195 |

配好Standard后,就在96孔板上加Standard和sample,习惯总量是25μl。所以Standard加25μl,分别加两次于一二排。而sample稀释十倍,所以是加2.5μl的sample和22.5μl的水,分别加三次于第三排往后的孔里。
加好Standard和sample后,便是加BCA reagent,是现配的,每200μl的Reagent A加4μl的Reagent B,混好后每个孔加200μl。加好后将96孔板放37℃里15-30分钟,就可以拿去测吸光度了🪄(可以看到蛋白浓度越高越紫,如上图的紫色),系统根据吸光度就可以算出sample的蛋白浓度。
蛋白浓度量好后就可以根据蛋白浓度准备sample跑Western blot了。每个sample都应根据测出的蛋白浓度取出等量的蛋白,比如有一个sample测出的浓度是2.942μg/μl,如果要取50μg出来的话就要取17μl = 50/2.942来准备sample。这样取完后,每个sample要再加一定量的lysis buffer让每个sample的体积相等。然后每个sample还要加总体积量1/4的4×SDS loadig dye。听着有点复杂😂,但可以做张表,按着表加就行了:
这里以总量40μl,蛋白量50μg为例
| Sample | Sample 1 | Sample 2 | Sample 3 |
|---|---|---|---|
| Conc. (μg/μl) | C1 | C2 | C3 |
| Vol (for 50μg) | 50/C1 | 50/C2 | 50/C3 |
| Lysis buffer (μl) | 40-10-50/C1 | 40-10-50/C2 | 40-10-50/C3 |
| Loading dye | 10μl | 10μl | 10μl |
| Total | 40μl | 40μl | 40μl |

配好的sample可以在室温里放很久,但别放到冰箱里,因为loading dye里是有SDS的,温度一降就会析出📉。
Sample要用前放到100℃里五分钟让蛋白变性,如上图所示,加水沸腾♨️然后放上sample,要刚好五分钟,太长太短都有可能导致Western blot失败。
Gel Preparation
| Gel Percentage | ddH₂O (ml) | Acrylamide/Bis (ml) | Gel Buffer (ml) | 10% SDS (ml) |
|---|---|---|---|---|
| 4% | 6.1 | 1.3 | 2.5 | 0.1 |
| 5% | 5.7 | 1.7 | 2.5 | 0.1 |
| 6% | 5.4 | 2 | 2.5 | 0.1 |
| 7% | 5.1 | 2.3 | 2.5 | 0.1 |
| 8% | 4.7 | 2.7 | 2.5 | 0.1 |
| 9% | 4.4 | 3 | 2.5 | 0.1 |
| 10% | 4.1 | 3.3 | 2.5 | 0.1 |
| 11% | 3.7 | 3.7 | 2.5 | 0.1 |
| 12% | 3.4 | 4 | 2.5 | 0.1 |
| 13% | 3.1 | 4.3 | 2.5 | 0.1 |
| 14% | 2.7 | 4.7 | 2.5 | 0.1 |
| 15% | 2.4 | 5 | 2.5 | 0.1 |
| 16% | 2.1 | 5.3 | 2.5 | 0.1 |
| 17% | 1.7 | 5.7 | 2.5 | 0.1 |
| *Resolving Gel buffer: 1.5M Tris-HCI, pH 8.8 | ||||
| *Stacking Gels Buffer: 0.5M Tris-HCI, pH6.8 | ||||
讲完Protein sample的准备后,接着就该讲讲怎么做胶了🙇♂️,咳咳。跑Western blot的胶叫SDS-PAGE,中文应该叫聚丙烯酰胺凝胶。胶分为上下两部分,下层是Resolving gel (分离胶),是胶的主体部分;上层是Stacking gel(浓缩胶),就是梳子的那个部分。
做胶前要先把玻璃板洗干净,洗到“一层水膜,既不聚成液滴,也不成股流下”(怎么感觉回到了初中化学😂)。洗好晾干后,前后玻璃板对齐好然后夹紧,要确保不漏液💦。我们一般习惯用1.5mm厚的,也有1mm厚或不同规格的,这样可以加载sample的量不一样。
准备好玻璃板后,就可以按照表中的配方配胶了📜,一般最常用的是8%,10%,12%的胶(如表中加粗),蛋白大点比如100kDa就用8%的胶,蛋白小点比如30kDa就用12%的胶,如果蛋白更小(<20kDa)就会用15%的胶。
Resolving gel按表中配方加H2O,acrylamide,gel buffer,和10%SDS后,还得再加100μl的20%APS和10μl的TEMED。APS和TEMED加下去后胶就会慢慢开始凝固了,所以动作不能拖拉,加完APS和TEMED晃均匀后就把胶倒到玻璃板间🫗,倒满整个主体,留一个梳子多一些的高度,大概就倒到图中绿色架子的那条线的地方。这时候上面可能会有些小泡泡🫧,所以在上面加一层甲醇,泡就消掉了。
等个十来分钟⌛️,可以看到管里刚才倒剩的液体凝固,然后就可以加stacking gel了。Stacking gel是按4%的胶配的,但gel buffer不一样,stacking gel用的是pH6.8的那个。倒stacking gel前记得先把刚才加的那层甲醇给倒掉,然后剩下的空间用stacking gel倒满。倒满后再把梳子插下去,这样就不会出现气泡问题了🫧。
加完stacking gel之后再等个十来分钟等胶完全凝固,好了后要把玻璃板上残留的胶给洗掉🚿,把梳子拔出来,把每个孔里残留的水给吸出来,就可以拿组装跑胶了。
如果做好的胶不马上用的话,可以用湿纸巾包住,然后外面用保鲜膜包好📩(防止胶干掉,没错,就是超市买的保鲜膜),放到4°C冰箱里。一般我最多就放个一晚上,隔天用,因为放久了胶发生什么变化谁也不知道🤷♂️。
图中是我做的胶,可以看到管里剩余的已经凝固成胶了,这时候就能洗洗拿去用了
做胶最容易出的问题一般是漏胶💦,一般是由于前一次做胶玻璃板下那块灰色的垫子没洗干净,上面还有凝固的小颗粒,导致玻璃板夹不紧,胶倒下去就从缝隙里流出来了。所以每次做完胶要尽快洗干净,不然下一个人做就会漏胶😬。

图中是我做的胶,可以看到管里剩余的已经凝固成胶了,这时候就能洗洗拿去用了
Gel Electrophoresis
有了sample做好胶之后就可以准备开始跑胶了🏃♀️。首先要把设备组装起来,胶先装到gel holder上然后再放到tank里加running buffer。组装这个也是要小心的,先把玻璃板插到gel holder上,然后再慢慢推上去,可以看到上面两个角玻璃凸出来的地方和gel holder上的橡胶压实了,再合上两边的锁 。这个力度得控制好👇,压得太用力玻璃很容易会碎掉。一个gel holder可以放两块胶,如果只跑一块胶另一边用一块塑料板代替。
如图所示圈出来的两个地方就是需要压实的,不然两块板之间的running buffer就会流出来,越跑越慢💨


组装好的gel holder cassette放到tank里,然后倒入running buffer🫗。两块板之间要倒满running buffer,然后tank里就倒到2gel的那条线(不管一块两块)。如果gel holder没组装好,板之间的running buffer就会流出来💦,就没法跑电泳了。这时候可以拿出来重新组装⟳,如果实在还不行的话,可以索性tank里倒满running buffer,就是4gel那条线的位置。但tank里倒满running buffer,板之间的液面其实还是不是完全满的,这样跑电泳就会慢很多🐌。
如图所示板之间的running buffer加得满满的,然后外面tank里加到2 gel那条线。
Running buffer的配方:
1L 1× Running buffer = 900ml ddH₂O + 100ml 10× Running buffer
8L 10× Running buffer = 242.4g Tris base +1152g Glycine + 400ml 20%SDS + ddH₂O → 8L
组装好设备后就可以加sample了,千万记得前面说的每个sample加之前在100℃里放五分钟!加的时候每个sample用细的吸管全吸出来,然后伸到每个well里加进去。这时候手一定要拿稳了✊,慢慢加进去,不然一搅动sample从well漂出来,well之间就互相contaminate了。
除了sample外还得加个ladder作为标记🪜,ladder的量是3μl,所以如果sample总量是40μl的话,就以3μl ladder + 27μl lysis buffer + 10μl loading dye作为ladder,让ladder的总量和sample一样。
加好sample后盖上盖子就可以开始跑了,记得红的对红的,黑的对黑的,不然就反着跑了😂。启动电源后可以看到板之间有泡泡往上漂🫧,那就是开始跑了。一般刚开始跑的时候电压为90或100V,跑一半的时候可以升高到110V,到后面可以再升高到120V⚡️。而且跑的时候板之间的液面会慢慢慢慢地降一小点,所以我会中途暂停往中间倒running buffer让它跑快点🏃。按上述电压的话,一般大概跑两个小时(不同浓度的胶速度不同)。

跑到loading dye从胶里出来到tank里就算完成了🔚,这时候记得及时关,不然继续跑就把里面的蛋白给跑没了,尤其是小分子量的蛋白。或者实在不放心,loading dye跑到底部可以停了,再把有loading dye部分的胶切掉,不过感觉这样跑出来的条带就会细一点,因为蛋白跑开的程度小点。
Protein Transfer to Membrane
转膜是Western blot最容易出问题的一步
1L 1× Transfer buffer = 200ml Methanol 700ml ddH₂O + 100ml 10× Transfer buffer
8L 10× Transfer buffer = 242.4g Tris base +1152g Glycine + ddH₂O → 8L
Blocking and Primary Antibody Incubation
Washing buffer配方:
8L 1× Washing buffer = 800ml 10× TBS buffer + 8ml Tween-20 + ddH₂O
先加水到7L多再加Tween-20,然后再加水到8L,不然直接往Tween-20里加水会整出一堆泡来
4L 10× TBS buffer = 96g Tris base +352g NaCl + 3.8LddH₂O, pH7.6
Secondary Antibody Incubation
Detection
持续更新中。。。Continuing…
Become our partner now and start turning referrals into revenue!
Share our link, earn real money—signup for our affiliate program!
Turn your traffic into cash—join our affiliate program!